Posted on | Saturday, January 8, 2011 | No Comments
Dengan menggunakan teori VSEPR maka kita dapat meramalkan bentuk geometri suatu molekul. Dalam artikel ini maka akan di contohkan menentukan bentuk geometri molekul XeF2, XeF4, dan XeF6. Diantara molekul-molekul tersebut ada yang memiliki pasangan elektron bebas dan ada yang tidak, jadi molekul-molekul tersebut adalah contoh yang bagus untuk lebih memahami teori VSEPR.
Pertama kita harus mementukan struktur lewis masing-masing molekul. Xe memiliki jumlah elektron valensi 8 sedangkan F elektron valensinya adalah 7.(lihat gambar dibawah)

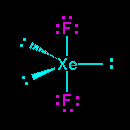
Struktur Lewis XeF2 seperti gambar sebelah kiri, dua elektron Xe masing-masing diapakai untuk berikatan secara kovalen dengan 2 atom F sehingga meninggalkan 3 pasangan elektron bebas pada atom pusat Xe. Hal yang sama terjadi pada molekul XeF4 dimana 4 elektron Xe dipakai untuk berikatan dengan 4 elektron dari 4 atom F, sehingga meninggalkan 2 pasangan elektron bebas pada atom pusat Xe.


Lihat gambar diatas XeF2 memiliki 2 pasangan elekktron terikat (PET) dan 3 pasangan elektron bebas (PEB) jadi total ada 5 pasangan elektron yang terdapat pada XeF2, hal ini menandakan bahwa geometri molekul atau kerangka dasar molekul XeF2 adalah trigonal bipiramid. Karena terdapat 3 PEB maka PEB ini masing masing akan menempati posisi ekuatorial pada kerangka trigonal bipiramid, sedangkan PET akan menempati posisi aksial yaitu pada bagian atas dan bawah. Posisi inilah posisi yang stabil apabila terdapat atom dengan 2 PET dan 3 PEB sehingga menghasilkan bentuk molekul linear. Jadi bentul molekul XeF2 adalah linier.(lihat gambar dibawah).

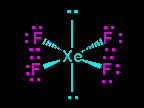
Lihat gambar strutur lewis XeF4 memiliki 4 pasangan elekktron terikat (PET) dan 2 pasangan elektron bebas (PEB) jadi total ada 6 pasangan elektron yang terdapat pada XeF4, hal ini menandakan bahwa geometri molekul atau kerangka dasar molekul XeF4 adalah oktahedral. Karena terdapat 2 PEB maka PEB ini masing masing akan menempati posisi aksial pada kerangka oktahedral, sedangkan PET akan menempati posisi ekuatorial. Posisi inilah posisi yang stabil apabila terdapat atom dengan 4 PET dan 2 PEB sehingga menghasilkan bentuk molekul yang disebut segiempat planar. Jadi bentul molekul XeF2 adalah segiempat planar.(lihat gambar dibawah).

Source
 Print halaman ini
Print halaman ini
Baca Juga Ini
Comments
Top Artikel
-
BAB I PENDAHULUAN A. Latar Belakang Perjalanan sejarah bangsa-bangsa di dunia menunjukkan bahwa kualitas sumber daya manusia terbukti s...
-
Tips ini berguna mungkin buat anda yang saat ini sedang berusaha untuk menghilangkan kebiasaan (ya mungkin boleh dikatakan kecanduan) nont...
-
Dengan sedikit trik, anda bisa merestart HP symbian teman anda tanpa harus melakukan kontak fisik ^_^ Anda bisa membuat kontes dengan teman-...
-
Sekering merupakan alat pengaman dari gangguan arus lebih ataupun hubung singkat. Di dalam beberapa sekering dipasang kawat perak sebagai ...
-
di matamu aku bukan siapa2, bukan teman, sahabat, bahkan saudara melainkan orang asing. namun biarlah orang asing ini singgah sejenak dal...
-
Tahukah anda, di saat anda terlelap malam tadi, bumi kita kejatuhan ribuan meteor? Fenomena itu sangat indah. Kilatan cahaya menghiasi langi...
-
1. Yahoo Melewatkan Facebook Tahukah Anda kalau Mark Zuckerberg pernah nyaris menjual hak kepemilikan Facebook kepada Yahoo? Tahun 2006, ...
-
Aktivasi otak tengah adalah suatu penemuan fenomenal dalam pendidikan anak. Teori penggunaan otak tengah sebenarnya telah banyak dilakukan...
-
Kesurupan bukan disebabkan oleh makhluk halus, tetapi reaksi kejiwaan yang diakibatkan tekanan sosial, kata peneliti dari Universitas Muhamm...
-
Suasana alam yang natural memang senantiasa memanjakan mata dan jiwa kita yang terkadang lelah dalam menjalani pekerjaan. Dalam suatu kesem...
Recent Post
Recent Comment
Categories
- Alam (1)
- Alien (5)
- Asal Usul (5)
- berita (1)
- Biografi (5)
- Budaya (30)
- Cerita Cinta (11)
- DOA (8)
- Fisika (21)
- Game Online (6)
- GAZA (3)
- Handphone (36)
- Indonesia (15)
- Islam (6)
- IT (14)
- Jejaring Sosial (1)
- kehidupan (2)
- Kesehatan (10)
- kimia (25)
- Komputer (40)
- kreasi (6)
- Materi Elektronika (21)
- Mencari Dollar (1)
- misteri (35)
- mitos (31)
- Otak (3)
- Otomotif (1)
- Pajak (4)
- Pendidikan (2)
- Penemuan (1)
- Pengen Tau? (16)
- psikologi (6)
- Puisi (2)
- Renungan Hati (8)
- Saint (1)
- Spiritual (22)
- Tentang Dunia Lain (25)
- Termodinamika (3)
- Tips (13)
- Tips Blogger (4)
- Tips Hidup (8)
- unique (7)
- Usaha (1)



Silahkan tuliskan komentar atau pertanyaan anda...!!!